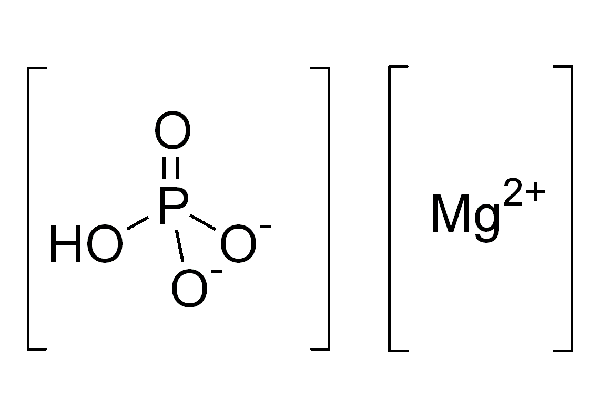
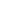Mghpo₄, 'n chemiese verbinding wat gereeld in chemie voorkom, veral in anorganiese chemie, is onder die naam bekend Magnesium waterstoffosfaat. Om die samestelling, eienskappe en gebruike van magnesiumwaterstoffosfaat te verstaan, is nodig om die chemiese elemente wat dit vorm, die molekulêre struktuur en die relevansie daarvan in verskillende velde, van nader te bekyk.
Verstaan die komponente van Mghpo₄
Om die benaming van MGHPO₄ te begryp, is dit noodsaaklik om die chemiese formule af te breek en die komponente te verstaan:
- Mg: Dit is die chemiese simbool vir magnesium, 'n metaalelement wat noodsaaklik is vir baie biologiese prosesse en wat wyd in verskillende industriële toepassings gebruik word. Dit is 'n alkaliese aardmetaal, geleë in groep 2 van die periodieke tabel, met 'n atoomgetal van 12.
- H: Dit staan vir waterstof, die ligste en volopste element in die heelal. Dit word dikwels in kombinasie met ander elemente aangetref en is 'n fundamentele bousteen van die lewe.
- Po₄: Dit verteenwoordig die fosfaatioon, 'n polyatomiese ioon wat bestaan uit een fosforatoom wat kovalent aan vier suurstofatome gebind is. Die algehele lading van 'n fosfaatioon (po₄³⁻) is -3, maar in die verbinding mghpo₄ verander die teenwoordigheid van waterstof die ioon na 'n waterstoffosfaatioon (HPO₄²⁻) met 'n lading van -2.
As hierdie komponente bymekaarkom om MGHPO₄ te vorm, word die verbinding magnesiumwaterstoffosfaat genoem, wat 'n aanduiding is van die teenwoordigheid van magnesium- en waterstoffosfaatione.
Die benaming van magnesiumwaterstoffosfaat
In chemiese nomenklatuur weerspieël die naam van 'n verbinding tipies die elemente en hul verhoudings daarin. Die naam magnesium waterstoffosfaat dui op die teenwoordigheid van magnesium (Mg), waterstof (H) en fosfaat (PO₄) in die verbinding. Hier is 'n uiteensetting van die naamkonvensie:
- Magnesium (Mg): Dit kom eerste in die naam, want dit is die metaal katioon met 'n +2 -lading.
- Waterstoffosfaat (HPO₄²⁻): Dit kom tweede en verteenwoordig die anioon wat bestaan uit waterstof en fosfaat. Die waterstof in hierdie konteks is nie 'n vrye element nie, maar 'n deel van die waterstoffosfaatioon, wat verskil van 'n fosfaatioon deur die teenwoordigheid van een addisionele waterstofatoom, wat die algehele negatiewe lading van -3 tot -2 verminder.
Deur hierdie naamkonvensies te volg, word die saamgestelde mghpo₄ akkuraat benoem Magnesium waterstoffosfaat.
Eienskappe van magnesium waterstoffosfaat
Magnesium waterstoffosfaat het verskillende noemenswaardige eienskappe wat dit nuttig maak in verskillende toepassings:
- Oplosbaarheid: Magnesium waterstoffosfaat is matig oplosbaar in water. Die oplosbaarheid daarvan is afhanklik van die pH van die oplossing en word meer oplosbaar in suuromstandighede. Hierdie eienskap is beduidend wanneer die gebruik daarvan in landbou- en mediese toepassings oorweeg word waar pH -vlakke kan wissel.
- Kristalstruktuur: Hierdie verbinding vorm tipies as 'n kristallyne vaste stof. Die kristalstruktuur kan afhang van die toestande waaronder dit gesintetiseer word, maar dit neem gewoonlik 'n struktuur aan wat die stabilisering van die waterstoffosfaatioon en magnesium moontlik maak.
- Stabiliteit: Magnesium -waterstoffosfaat is stabiel onder normale omstandighede, maar kan ontbind as dit tot hoë temperature verhit word, en in magnesiumpirofosfaat en water afbreek.
Gebruike en toepassings van magnesium waterstoffosfaat
Magnesium waterstoffosfaat het verskeie belangrike toepassings oor verskillende velde as gevolg van die chemiese eienskappe daarvan:
- Landbou: In die landbou word magnesiumwaterstoffosfaat as kunsmis gebruik. Fosfate is noodsaaklike voedingstowwe vir plante, wat wortelontwikkeling en blom bevorder. Die magnesiumkomponent is ook voordelig, aangesien dit 'n kritieke element in chlorofil is, wat help met fotosintese en algehele plantgesondheid.
- Medies en farmaseuties: In die mediese veld word magnesiumwaterstoffosfaat soms gebruik as 'n voedingsaanvulling om tekortkominge in magnesium en fosfor aan te spreek. Magnesium is van kardinale belang vir verskillende liggaamsfunksies, insluitend spier- en senuwee -funksie, bloedsuikerbeheer en bloeddrukregulering. Fosfate is noodsaaklik vir die vorming van been- en tande, sowel as energieproduksie.
- Voedselbedryf: Dit word as toevoeging in die voedselbedryf gebruik, en dien dikwels as 'n suurdeeg in die bak. Dit kan ook dien as 'n suurreguleerder en 'n mineraalaanvulling in verskillende voedselprodukte.
- Waterbehandeling: Magnesium waterstoffosfaat kan in waterbehandelingsprosesse gebruik word, veral in die verwydering van swaar metale en ander kontaminante. Die verbinding kan help met die neerslag van ongewenste ione, wat help om water te suiwer.
Konklusie
Magnesium -waterstoffosfaat (MGHPO₄) is 'n veelsydige verbinding met 'n wye verskeidenheid toepassings in landbou, medisyne, voedsel en waterbehandeling. Die begrip van die samestelling daarvan, eienskappe en gebruik daarvan beklemtoon die belangrikheid van hierdie verbinding in beide industriële en alledaagse kontekste.
Deur die naam en komponente van MGHPO₄ af te breek, sien ons hoe die nomenklatuur die aanwesige elemente en hul onderskeie ladings weerspieël. Hierdie duidelikheid in die benaming is van kardinale belang vir die behoorlike identifisering en toepassing van chemiese verbindings in verskillende velde, wat verseker dat magnesium -waterstoffosfaat korrek benut word om meerdere nywerhede en verbruikers te bevoordeel.
Postyd: Aug-29-2024